Una reacción química está presente cuando una o más sustancia se transforman en otras diferentes. En otras palabras, al mezclar elementos o sustancias, estas van a producir una nueva sustancia. Las reacciones químicas se representan gráficamente con una ecuación química la cual específica los elementos o sustancias involucrados en la reacción química.
En una ecuación química están presentes los reactantes, localizados en la parte izquierda de la flecha y los productos, que se encuentran en la parte derecha. Algunas ecuaciones químicas también pueden indicar los estados (solido, liquido, gaseoso) en los que se encuentran los reactantes y productos que pueden ser: (s) solido, (l) liquido, (g) gaseosos y (ac) solución acuosa.
Para que un reactante actúe en una reacción química es necesaria la intervención de un catalizador, temperatura o condiciones especiales necesarias en la reacción.
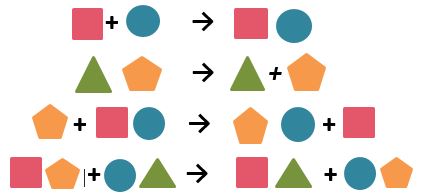
A continuación se muestran los cuatro tipos de reacciones químicas mas comunes:
a) Reacción de síntesis o composición: Los elementos que se combinan en esta reacción son el litio y el óxido se juntan para formar oxido de litio.
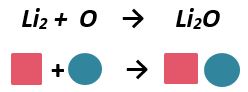
b) Reacción de descomposición o análisis: En este tipo de reacción un compuesto se descompone en los elementos que lo forman. Así tenemos que el óxido de Potasio se separa en sus dos elementos el Potasio y el Oxígeno.
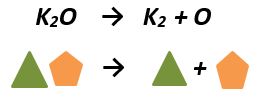
c) Reacción de desplazamiento o sustitución sencilla: en esta reacción un elemento desplaza a otro en un compuesto para formar uno diferente. El Zinc es un metal más activo que el cobre por lo que lo desplaza para formar sulfato de zinc dejando libre al cobre como producto de la reacción.
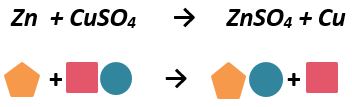
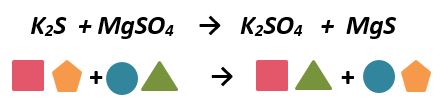
d) Reacción de doble desplazamiento o intercambio: En esta reacción hay un intercambio entre los dos compuestos, el Sulfuro de Potasio y el Sulfato de Magnesio.

Hola mi nombre es cristela
Hola mi nombre es cristela
y acabo de pasar todos Los examenes del GED. quiero dar las gracias a Luz por su Apoyo para pasar el que se me dificultaba mas que es de matematicas les recomiendo usar el curso que a mi me ayudo a pasarlo que es el curso de matematicas que tienen a la venta el cual contiene examenes de practica con videos explicando cada respuesta. Gracias a ti Luz puede pasarlo. Gracias
FELICIDADES!!!
MUCHAS FELICIDADES!!!! Cristela. Me da mucho gusto saberlos, espero que sea uno de muchos logros. Saludos!!
GED
Hola, mi nombre es Erka y megustaria tener conocimientos a cerca de ciencia,
estoy estudiando GED. me gustaria contar con su apoyo le agradezco mucho.
Bonito dia.
Para el examen de ciencias
Para el examen de ciencias debes tener conocimiento generales de biología, química, física y ciencias de la tierra. No te van a preguntar nada que no este en el texto, ilustraciones, tablas u otras fuentes de información. Creo que los contenidos mas dificiles son los de química y física aunque todo depende de cada estudiante. Aquí te dejo algunos contenidos que puedes revisar, no te limites a estos, trata de conseguir o alquilar un libro en la biblioteca y repasa los exámenes de practica. Saludos!!
BIOLOGIA
Célula
https://www.spanishged365.com/72/la-celula
ADN
https://youtu.be/NQaZecHCCNA
Sistemas en el cuerpo humano
https://youtu.be/D-XfciuMdYs
cromosomas y genes
https://www.spanishged365.com/111/cromosomas
Neurosis
https://www.spanishged365.com/112/neuronas
Celulas madre
https://www.spanishged365.com/380/celulas-madre
Recursos BIOLOGIA
https://www.spanishged365.com/363/recursos-didacticos-biologia
Leyes de Mendel
http://recursostic.educacion.es/secundaria/edad/4esobiologia/4quincena6/4quincena6_contenidos_1a.htm
meiosis mitosis
https://youtu.be/p8ckQO-yFN4
https://youtu.be/3TqmT1-OSp8
https://youtu.be/2p4H1JHo1lk
Origen de la vida
https://youtu.be/ClUevS7bKl0
https://youtu.be/eTdm4gHfSOY
https://youtu.be/GrMh-IkFMUE
https://youtu.be/GrMh-IkFMUE minuto 16
Evolution
https://youtu.be/U3CfkHUCsR0
https://youtu.be/knMKUyfPDk8
QUIMICA
Atomos
https://www.youtube.com/watch?v=ezgUFdUgpzA
https://www.youtube.com/watch?v=-6PpDBTyZ28
MOLECULAS
https://www.youtube.com/watch?v=ezgUFdUgpzA
ecuación química
https://youtu.be/rbYK5Ig-oXU
Balanceo de ecuaciones
https://youtu.be/Ql4zJI5ZMxA
Ecuaciones químicas
https://www.spanishged365.com/371/balanceo-de-ecuaciones-quimicas
Reacciones químicas
https://www.spanishged365.com/386/reacciones-quimicas
Encale covalente
https://www.spanishged365.com/121/enlace-covalente
Enlace ionico
https://www.spanishged365.com/120/enlace-ionico
Recursos didácticos / aquí pueden estudiar varios recursos de química, como la tabla periódica, balanceo de ecuaciones, diferencia entre sustancias, mezclas, etc.https://www.spanishged365.com/362/recursos-didacticos-quimica